Электролитическая диссоциация. Электролиты
Автор статьи — профессиональный репетитор И. Давыдова (Юдина).
Электрический ток – направленное движение заряженных частиц – электронов или ионов.
В 1887 г. шведский ученый Сванте Аррениус, изучая электропроводность растворов различных веществ, пришел к выводу, что причиной электропроводности является наличие в растворе ионов, которые образуются при растворении электролита в воде. Процесс распада электролита на ионы называют электролитической диссоциацией.
Сведения об электролитической диссоциации отражены в Теории электролитической диссоциации (ТЭД):
1. При растворении в воде электролиты распадаются (диссоциируют) на две заряженные частицы. Положительная называется катионом, отрицательная – анионом (по составу ионы подразделяют на простые – Na+, Ba2+, Cl–, S2– и сложные – NO3–, SO42–, PO43–, NH4+, CH3COO–).
2. Причиной диссоциации электролита в водном растворе является его гидратация (взаимодействие электролита с молекулами воды).
3. Под действием электрического тока катионы движутся к отрицательному полюсу источника тока – катоду, а анионы движутся к положительному полюсу источника тока – аноду. Растворы электролитов электронейтральны, т.к. сумма зарядов катионов равна сумме зарядов анионов.
4. Диссоциация обратимый процесс для слабых электролитов. Наряду с процессом диссоциации (распад на ионы) протекает и обратный процесс – ассоциация (соединение ионов). Поэтому в уравнениях электролитической диссоциации для слабых электролитов используют знак обратимости ”⇄”, а для сильных – знак равенства “=” или односторонюю стрелочку “→”.
5. Электролиты диссоциируют по-разному, в разной мере. По степени диссоциации электролиты подразделяются на слабые и сильные.
6. Химические свойства растворов электролитов определяются свойствами тех ионов, которые они образуют при диссоциации. Кислоты при диссоциации образуют катионы водорода (Н+) и анионы кислотного остатка, основания образуют катионы металла и анионы гидроксогрупп (OH–), соли образуют катионы металла и анионы кислотных остатков.
Электролиты – это вещества, растворы или расплавы (в ОГЭ и ЕГЭ чаще речь о растворах) которых проводят электрический ток, то есть содержат заряженные частицы. Свободных электронов в растворе не бывает, носителями заряда являются ионы. Электрический ток проводят расплавы веществ с ионной кристаллической решеткой.
К электролитам относятся:
Чем больше в растворе заряженных частиц, тем лучше он проводит электрический ток, т.е. чем больше молекул вещества диссоциирует, тем более сильным электролитом оно является.
Список сильных и слабых электролитов нужно знать наизусть!
Сильные электролиты (в растворах):
NaCl, FeCl3, KHCO3, CuSO4, K2CO3, (CH3COO)2Ba, NaH2PO4 и т.д.
8 растворимых гидроксидов: LiOH, NaOH, KOH, RbOH, CsOH, Ba(OH)2, Sr(OH)2, Ca(OH)2.
HI, HBr, HClO4, HCl, H2SO4(разб), HMnO4, HNO3, HClO3.
Слабые электролиты:
нерастворимые основания (Mg(OH)2, Cu(OH)2, Fe(OH)2, Mn(OH)2), в т.ч. амфотерные гидроксиды (Al(OH)3, Cr(OH)3, Fe(OH)3, Pb(OH)2, Zn(OH)2, Be(OH)2), гидроксид аммония, т.е. гидрат аммиака (NH3⦁H2O) и растворы аминов.
- Слабые кислоты и кислоты средней силы
HClO2, H2SO3, H3PO4, HF, HNO2, H2CO3, H2S, HClO, HCN, H2SiO3, CH3COOH и другие органические кислоты.
H2O – очень слабый электролит, диссоциирует ничтожно мало. Чистая дистиллированная вода не проводит электрический ток.
Неэлектролиты: оксиды, большинство органических соединений, а также вещества, в молекулах которых имеются только ковалентные неполярные или малополярные связи и т.д.
Сила электролита определяется степенью диссоциации. Степень диссоциации обозначают греческой буквой α, она рассчитывается по формуле:
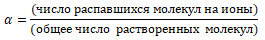
Степень электролитической диссоциации может иметь значение от 0 до 1 (в процентах от 0 до 100%). Если α = 0, то диссоциация отсутствует, а если α = 1, то электролит полностью распадается на ионы. Иногда α переводят в проценты для удобства восприятия. Тогда формула будет выглядеть так:
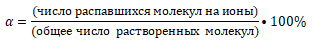
Электролитом считают вещества со степенью диссоциации от 40% и выше. Про такие вещества говорят, что они сильные электролиты. Про вещества со степенью диссоциации менее 40% говорят, что они слабые электролиты. Вещества совсем неспособные распадаться называют неэлектролитами.
Чтобы понять, какие ионы образуются при распаде электролита, следует обратиться к таблице растворимости. Попробуем составить уравнения диссоциации некоторых веществ.
Рассмотрим соль А2В и кислоту Н3Х:
Соли диссоциируют почти на 100%:
А2В → 2А+ + В2–. Так как все молекулы распались на ионы, из 1 моль А2В получилось 1 моль В2– и 2 моль А+, то есть три моль ионов.
Многоосновные кислоты диссоциируют ступенчато:
Н3Х ⇄ H++H2X– (1 ступень)
Н2Х–⇄H++HX2– (2 ступень)
HX2–⇄H++X3– (3 ступень)
При этом каждая следующая ступень диссоциации протекает хуже (слабее) предыдущей, т.к. присутсвует конкурирующий процесс – обратная реакция. Порядок примерно такой: Из 1 моль молекул слабой кислоты по первой ступени диссоциировало 0,05 моль, по второй – 0,0002 моль и по третьей – 0,00000001 моль. Итого образовалось чуть больше 0,1 моль ионов.
Очевидно, этот раствор этой кислоты проводит ток хуже, чем раствор соли.
Теперь рассмотрим на конкретных примерах диссоциацию кислот, солей и оснований.
Кислоты
1. Одноосновные сильные кислоты (сильные электролиты) диссоциируют необратимо нацело: HCl → H+ +Cl– (одна ступень)
HNO3 → H+ +NO3– (одна ступень)
HClO4 → H+ +ClO4– (одна ступень)
2. Одноосновные слабые кислоты диссоциируют обратимо нацело:
HF ⇄H+ + F– (одна ступень)
HCN ⇄H+ + CN– (одна ступень)
HNO2⇄H+ +NO2–(одна ступень)
3. Многоосновные сильные кислоты (сильные электролиты) диссоциируют следующим образом:
Серная кислота (двухосновная кислота) диссоциирует:
H2SO4 → H+ + HSO4– (первая ступень)
HSO4–⇄H+ + SO42– (вторая ступень)
Поскольку серная кислота является сильной, то её уравнение диссоциации, как правило, отражают в одну ступень:
H2SO4 → 2H+ + SO42–
4. Многоосновные слабые кислоты диссоциируют обратимо и ступенчато:
Сероводородная кислота (двухосновная кислота) диссоциирует:
H2S⇄H+ + HS–(первая ступень, образование гидросульфид-ионов)
HS-–⇄H+ + S2–(вторая ступень, образование сульфид-ионов)
Ортофосфорная кислота (трехосновная кислота) диссоциирует:
H3PO4⇄H+ +H2PO4–(первая ступень, образование дигидрофосфат-ионов)
H2PO4-⇄H+ +HPO42–(вторая ступень, образование гидрофосфат-ионов)
HPO42-⇄H+ +PO43–(третья ступень, образование фосфат-ионов)
Основания
1. Растворимые основания – щелочи (сильные электролиты) диссоциируют необратимо нацело:
а) Однокислотные:
NaOH → Na+ + OH–
KOH → K+ + OH–
RbOH → Rb+ + OH–
б) Многокислотные:
Ba(OH)2→ Ba2+ + 2OH–
2. Растворимое слабое основание гидроксид аммония (водный раствор аммиака) диссоциирует обратимо:
NH3⦁H2O⇄NH4++ OH–
Примечание: вместо записи “NH3⦁H2O” допускается запись “NH3+ H2O”.
3. Нерастворимые многокислотные основания диссоциируют обратимо и ступенчато:
Гидроксид меди (II) (двухкислотное основание) диссоциирует:
Cu(OH)2⇄CuOH+ + OH– (первая ступень)
CuOH+⇄Cu2+ + OH– (вторая ступень)
Поскольку это нерастворимое основание (не растворяется в воде), то реально уравнение диссоциации отражает процесс только тогда, когда мы добавляем к нерастворимому основанию раствор кислоты.
Амфотерные гидроксиды
Амфотерные гидроксиды это слабые электролиты, которые диссоциируют одновременно и как основание, и как кислота, т.е при диссоциации образуют одновременно катион водорода (Н+) и анионы гидроксогрупп (OH–).
Me(OH)n⇔ HnMeOn
Например, амфотерный гидроксид цинка можно записать и в виде основания (гидроксид цинка), и в виде кислоты (цинковая кислота):
Zn(OH)2⇔ H2ZnO2
Диссоциация по типу основания: Me(OH)n⇄Men+ + nOH–.
Zn(OH)2⇄ZnOH+ + OH– (первая ступень)
ZnOH+ ⇄Zn2+ + OH– (вторая ступень)
Диссоциация по типу кислоты: HnMeOn⇄nH+ + MeOnn– .
H2ZnO2⇄H+ + HZnO2– (первая ступень)
HZnO2– ⇄H++ ZnO22– (вторая ступень)
НО! Поскольку амфотерные гидроксиды это нерастворимые в воде вещества, то реально уравнение диссоциации отражает процесс только тогда, когда мы добавляем к амфотерному гидроксиду или раствор щелочи, или раствор кислоты.
Соли
Средние (нормальные) соли
Средние (нормальные) соли являются сильными электролитами, диссоциируют необратимо нацело. Примеры:
KBr → K++ Br–
AgNO3→ Ag+ +NO3–
NH4Cl → NH4++Cl–
AlI3→ Al3+ + 3I–
Sr(NO2)2→ Sr2+ + 2NO2–
Na2CO3→ 2Na++ CO32–
Cu(NO3)2→ Cu2+ + 2NO3–
Al2(SO4)3→ 2Al3+ + 3SO42–
LiClO3→ Li+ + 3ClO3–
K3PO4→ 3K+ + PO43–
Fe(ClO4)2→ Fe2+ + 2ClO4–
(CH3COO)2Pb → Pb2+ + 2CH3COO–
Кислые соли
Кислые соли являются сильными электролитами, диссоциируют ступенчато.
а) если кислая соль образована слабыми многоосновными кислотами:
Гидрокарбонат натрия диссоциирует:
NaHCO3→ Na+ + HCO3– (первая ступень, диссоциация необратимая, α = 1).
HCO3–⇄ H+ + CO32– (вторая ступень, диссоциация обратимая, α < 1).
Гидрофосфат аммония диссоциирует:
(NH4)2HPO4→ 2NH4++ HPO42– (первая ступень, диссоциация необратимая, α = 1).
HPO42–⇄H++PO43– (вторая ступень, диссоциация обратимая, α < 1).
Оснóвные соли
Оснóвные соли являются электролитами, диссоциируют ступенчато.
Дигидроксохлорид алюминия диссоциирует в три ступени:
Al(OH)2Cl → Al(OH)2++ Cl–(первая ступень, диссоциация необратимая, α = 1).
Al(OH)2+⇄AlOH2++ OH– (вторая ступень, диссоциация обратимая, α < 1).
AlOH2+⇄Al3++ OH– (третья ступень, диссоциация обратимая, α < 1).
Несколько вопросов для тренировки:
1) Какие частицы образутся при диссоциации нитрата натрия?
а) Na+, N+5, O-2;б) Na+, NO3–; в) Na, NO2, O2; г) NaNO2, O2
Решение:
Нитрат натрия образован остатком азотной кислоты и катионом натрия. Уравнение его диссоциации: NaNO3→ Na+ + NO3–.
Ответ: б).
2) В четырех пробирках находятся одномолярные растворы следующих веществ:
а) H3PO4 б) Na2SO4 в) NaCl г) HF
В какой пробирке больше всего ионов?
Решение:
a) ортофосфорная кислота – средней силы, диссоциирует слабо, большая часть молекул останутся в растворе молекулами, а не ионами.
б) сульфат натрия – соль, диссоциирует полностью, из одного моль соли получается три моль ионов: Na2SO4 → 2Na+ + SO42–.
в) хлорид натрия – соль, диссоциирует полностью, из одного моль соли образуется два моль ионов: NaCl → Na+ + Cl–.
г) фтороводородная (плавиковая) кислота – слабая кислота, диссоциирует слабо, большая часть молекул останутся в растворе молекулами, а не ионами.
Ответ: б).
3) Выберите два вещества, которые не являются электролитами.
а) парафин;
б) хлороводород;
в) поваренная соль;
г) углекислый газ;
д) гидроксид лития.
Решение:
а) парафин – это органическое вещество, относящееся к углеводородам. Такое вещество электролитом не является. Этот вариант ответа нам подходит.
б) хлороводород – при растворении в воде превращается в хлороводородную (соляную) кислоту, она является сильной кислотой, сильным электролитом и диссоциирует необратимо нацело: HCl → H+ +Cl– .
в) поваренная соль – это вещество по-другому называется хлорид натрия. Это средняя соль и сильный электролит, который диссоциирует в растворах необратимо нацело:
NaCl → Na+ + Cl–.
г) углекислый газ – является оксидом. Оксиды электролитами не являются. Этот вариант ответа нам подходит.
д) гидроксид лития – растворимое однокислотное основание (щелочь), является сильным электролитом и диссоциирует необратимо нацело: LiOH → Li+ + OH– .
Ответ: а) и г).
4) Выберите два вещества, при полной диссоциации 1 моль которых образуется 3 моль анионов.
а) AgNO3;б) Fe2(SO4)3; в) Ba(NO2)2; г) KClO4; д) Al(NO3)3.
Совет: внимательно читаем задание, внимательно смотрим на то, что нам нужно найти. В данном случае нам нужно найти 3 моль именно анионов, а не всех ионов вместе!
Решение:
Напишем уравнения диссоциации каждого вещества:
а) AgNO3→ Ag+ +NO3– (образуется 1 моль нитрат-анионов. Не подходит).
б) Fe2(SO4)3→ 2Fe3+ + 3SO42– (образуется 3 моль сульфат-анионов. Подходит).
в) Ba(NO2)2→ Ba2+ + 2NO2– (образуется 2 моль нитрит-анионов. Не подходит).
г) KClO4→ K+ + ClO4– (образуется 1 моль перхлорат-анионов. Не подходит).
д) Al(NO3)3→ Al3+ + 3NO3– (образуется 3 моль нитрат-анионов. Подходит).
Ответ: б) и д).
Литература:
1. Егоров А.С. Готовимся к экзамену по химии. Для поступающих в средние специальные учебные заведения. – Ростов н/Д: Феникс, 2005. – (Абитуриент).
2. Габриелян О.С. Химия. 8 класс: учеб. для общеобразоват. учреждений. – М.: Дрофа, 2006.
3. ОГЭ. Химия: типовые экзаменационные варианты: 30 вариантов / под ред. Д.Ю.Добротина. – М.: Издательство “Национальное образование”, 2023. – (ОГЭ. ФИПИ - школе).